به هر ماده شیمیایی که از ترکیب سه عنصر فسفر، اکسیژن و هیدروژن (در نسبتهای مختلف) ساخته شده باشد، اسید فسفریک میگویند. ارتو فسفریک اسید رایجترین نوع اسید فسفریک با فرمول شیمیایی H۳PO۴ است که نام ساده این اسید است. در عین حال دو مولکول این ترکیب از واکنش شیمیایی سه مولکول آب با دو مولکول پنتا اکسید فسفروس حاصل میشود. این ترکیب کریستالهای لوزی شکل به وجود میآورد.
کریستالها در دمای حدود ۴۲ درجه سانتیگراد ذوب میشوند و وزن مخصوصی برابر ۱,۸۳۴ گرم بر سانتیمتر مکعب در دمای ۱۸ درجه سانتیگراد پیدا میکنند. این اسید یکی از پرکاربردترین اسیدها در صنایع دارویی، غذایی، آرایشی و علیالخصوص کشاورزی است. در نتیجه آشنایی با تاریخچه، خواص و کاربردهای آن برای اهل فن و علاقمندان ضروری است.
فهرست محتوا
اسید فسفریک چیست؟
اسید فسفریک یک اسید معدنی با فرمول شیمیایی H₃PO₄ است که از ترکیب سه عنصر فسفر، اکسیژن و هیدروژن تشکیل شده است. این اسید بیرنگ، بدون بو و معمولاً به صورت مایع چسبناک یا جامد کریستالی سفید موجود است. اسید فسفریک بهعنوان یکی از اسیدهای پرکاربرد در صنایع مختلف شناخته میشود و دارای خواص فیزیکی و شیمیایی ویژهای است.
تاریخچه اسید فسفریک
مشخص نیست که اسید فسفریک توسط چه کسی و در چه زمانی برای اولین بار کشف شده، اما مدارک ثبت شده در تاریخ اولین اختراع فسفر را به کارهای کیمیاگری آلمانی مربوط میکنند. این مدارک نشان میدهد که هننیگ برندت کیمیاگر و بازرگان قرن هفدهم میلادی و اوایل قرن هجدهم (۱۶۳۰-۱۷۱۰ میلادی) در هامبورگ آلمان، موفق به کشف فسفر در سال ۱۶۶۹ شد. مانند بقیه کیمیاگران آن زمان، برندت که به دنبال سنگ کیمیا بود کشفش را بهصورت یک راز حفظ کرد. او سعی کرد با استفاده از فسفر، طلا تولید کند که مسلماً موفق نشد.
طبق یادداشتهایی که بعد از مرگ او به جا مانده، مشخص نشد که آیا برندت در آزمایشهای خود با آب (کیمیاگران علاقه بسیاری به استفاده از ترکیب آب با مواد مختلف داشتند) موفق به تولید فسفریک اسید شده و یا خیر. تولید و کشف رسمی اسید فسفریک تا دهه ۱۷۷۰ طبق شواهد رسمی عقب افتاد.
تا دو شیمیست سوئدی به نامهای یوهان گاتلیب گان و کارل ویلهم شیل کاملاً مستقل از یادداشتهای برندت و از خاکستر استخوان موفق به تولید اسید فسفریک شدند. شیل در سال ۱۷۷۴ موفق به جداسازی فسفر از خاکستر استخوان شد و در سال ۱۷۷۷ با اضافه کردن اسید نیتریک به فسفر، موفق به تولید اسید فسفریک شد. برخی از منابع تولید اولیه اسید فسفریک را در سال ۱۶۹۴ توسط رابرت بویل با انحلال پنتا اکسید فسفر در آب تأیید کردهاند.
در سال ۱۸۱۲ در لیون فرانسه شرکت کویگنت موفق به کشف راهی برای تولید فسفر خالص با اضافه کردن اسید هیدروکلریک به استخوان شد. البته تا سال ۱۸۷۲ به صورت کامل تولید آن در اختیار دولت فرانسه قرار داشت و در ضمن اسید فسفریک به همراه محصولات دیگر فسفر تهیه میشد. این دانشمند در همین کتاب به فسفات غیر قابل انحلال موجود در استخوانها و مواد معدنی اشاره کرد و گفت که با واکنش این فسفات با اسید سولفوریک میتوان به ترکیبی مغذی برای گیاهان دست یافت.
در سال ۱۸۹۶ تمام استخوانهای بوفالوها از دشتهای آمریکا به دلیل تولید فسفر، اسید فسفریک و بقیه محصولات فسفردار از بین رفت. شرکتها به فکر جایگزین کردن استخوان با منبعی قابل اطمینانتر افتادند و به همین علت به استفاده از سنگهای معدنی فسفاته روی آورده شد. اما قبل از آن به دلیل گران شدن استخوان، بسیاری از آن افراد ورشکست شده بودند. اسید فسفریک امروزه از سنگهای فسفاته به دو روش کلی مرطوب (تر) و خشک تهیه میشود.

خواص اسید فسفریک چیست؟
خواص فیزیکی و شیمیایی اسید فسفریک به شرح زیر است:
خواص فیزیکی اسید فسفریک
اسید فسفریک خالص کریستالهای جامد سفید رنگی با درجه ذوب ۴۲,۳۵ درجه سانتیگراد هستند. این اسید در ۱۵۸ درجه سانتیگراد میجوشد و از هم تفکیک میشوند. وقتی که اسید فسفریک کمتر غلیظ شده باشد بیرنگ، بدون بو و بهصورت مایع چسبناکی با چگالی ۱.۶۸۵ گرم بر میلیلیتر در دمای اتاق است. البته مقدار این حجم و چگالی در هنگام جامد بودن برابر با ۲.۰۳ گرم بر میلیلیتر است.
این اسید غیرسمی است و قابل اشتعال نیست. بالاترین غلظت برای اسید فسفریک در آب ۸۵ درصد و کمترین مقدار آن برای فروش ۵۰ درصد است. بهترین دما برای نگهداری این اسید دمای 30 درجه سانتیگراد است. در دماهای پایینتر از ۲۰ درجه، این اسید بهصورت مایع بسیار سرد درمیآید و در بسیاری از مواقع منجمد نمیشود.
خواص شیمیایی اسید فسفریک
اسید فسفریک سه اتم هیدروژن اسیدی و قابل جایگزین دارد و به همین دلیل نسبت به دیگر اسیدهای معدنی متفاوت عمل میکند. فسفریک اسید توانایی واکنش با بازها برای تشکیل سه کلاس از نمکها را با جایگزین کردن یک، دو و یا هر سه اتم هیدروژن را دارا است.
یکی از تواناییهای کمیاب و جالب این اسید این است که در درجه حرارتهای بالا، مولکولهای اسید فسفریک قادر به واکنش با یکدیگر و ترکیب شدن (با از دست دادن مولکول آب) برای تشکیل زنجیرههای پلیمری کوتاه و حتی طولانی مانند پلی فسفریک اسید و متافسفریک اسید هست. باید توجه داشت که این اسید در واکنش با الکلها، آلدهیدها، سیانیدها، کتونها، فنولها، استرها، سولفیدها تجزیه میشود و بخار سمی تولید میکند.

فرآیند تولید فسفریک اسید
اسید فسفریک به دو روش حرارتی و روش تر تولید میشود. روش حرارتی محصولی با درجه خلوص بالا تولید میشود و قیمت تمام شده آن نیز نسبت به روش مرطوب (تر) بسیار بالاتر است. فسفریک اسید تولید شده به روش تر، بیشتر برای تولید کودهای شیمیایی و خوراک طیور به کار میرود و البته از طریق تصفیه این اسید میتوان آن را برای گرید خوراکی مناسب کرد.
نحوه تولید اسید فسفریک به روش حرارتی یا خشک
در این روش فسفر بهعنوان عنصری در مجاورت هوای اضافی به اکسید فسفر تبدیل میشود. این اکسید با جذب گرما و حرارت نهان سوخت و هیدراته شدن، اسید فسفریک تولید میکند. اما نکته قابل توجه اینجاست که غلظت اسید حاصل به میزان آب مصرف شده و میزان قدرت خنککنندگی سیستم وابسته است.
برای خنک کردن محفظه احتراق از روشهای مختلفی مانند دیواره خیس، دیواره خنک شونده با آب و دیواره خنک شونده با هوا میتوان استفاده کرد. در روش دیواره خیس، جریانی از اسید سرد شده از بالای محفظه احتراق به سمت پایین وجود دارد که باعث محافظت از آن میشود. در روش خنک شونده توسط هوا نیز محفظه احتراق از جنسهای نسوز مانند گرافیت یا آلومینا است و حرارت از طریق تشعشع و جابهجا شدن محفظهها خارج میشود.
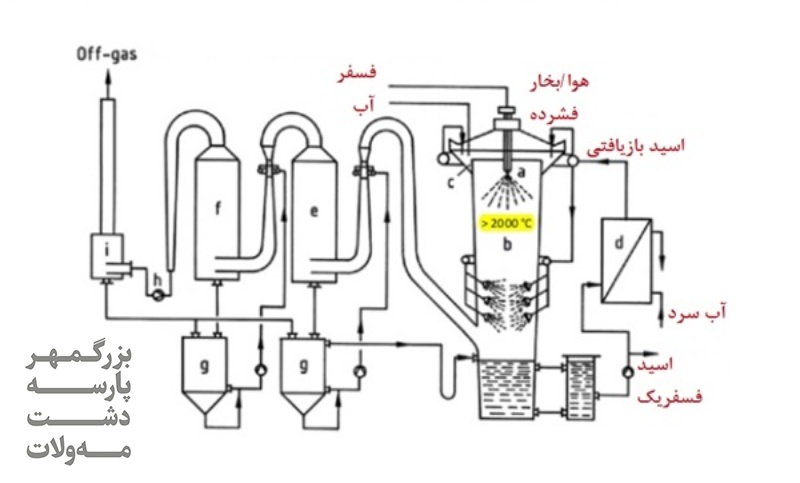
تولید اسید فسفریک به روش مرطوب یا تر
متداولترین روش تولید اسید فسفریک در جهان روش مرطوب یا تر است که در آن ماده اولیه سنگ معدن است و تولید در حجم بالا و درجه خلوص پایین انجام میپذیرد. در روش مرطوب یا تر از واکنش سنگ فسفات استخراج شده و خرد کردن آن با اسید سولفوریک، فسفریک اسید و گچ حاصل میشود. البته این سنگ به شکل فلوئور و آپاتیت است.
در اثر واکنش فسفریک اسید با سنگهای خرد شده فسفات در روش مرطوب، مونو کلسیم فسفات به وجود میآید. مونو کلسیم فسفات با اسید سولفوریک ترکیب و اسید فسفریک و گچ تولید میشود. با توجه به اینکه سنگهای فسفات ناخالصیهای گوناگونی دارند، در این فرایند واکنشهای جانبی متفاوتی اتفاق میافتد که باعث مصرف بیشتر اسید سولفوریک میشود.
اسید فسفریک تولید شده به روش تر به دلیل وجود ناخالصیهای حاصل از سنگ معدن، رنگی سیاه پیدا میکنند و مناسب برای مصارفی است که درصد خلوص اسید اهمیت چندانی ندارد. فرایندهای دی هیدرات، همی هیدرات و انیدرید جزو روشهای تهیه اسید فسفریک بهصورت مرطوب یا تر هستند و هر کدام از این فرایندها مزایا و معایب خود را دارند.
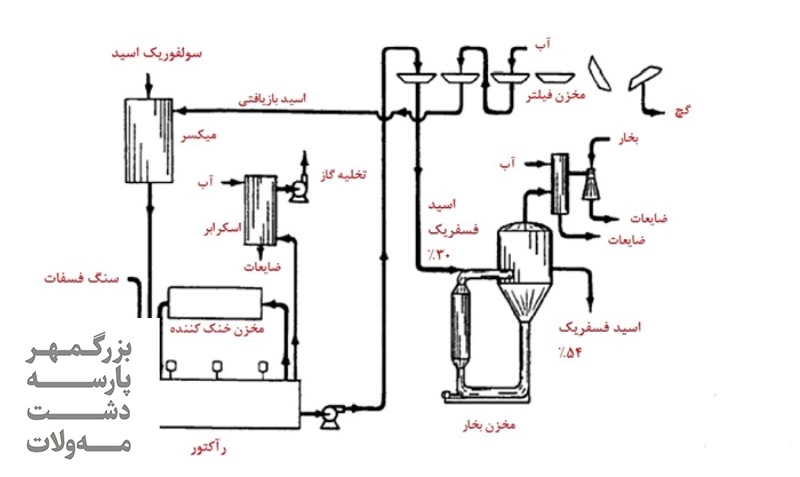
خالصسازی اسید فسفریک تولید شده در روش مرطوب یا تر چگونه است
همانطور که گفته شد اسید حاصل از روش تر درصد خلوص پایینی دارد و به همین دلیل برای استفاده در صنایع غذایی نمیتواند مناسب باشد. برای اینکه بتوان از فسفریک اسید تولید شده به روش مرطوب در گرید خوراکی نیز استفاده کرد، باید فرایند خالصسازی را در نظر گرفت. روشهای مختلفی برای انجام وجود دارد که در زیر به برخی از آنها اشاره میکنیم.
- شفافسازی: اسید فسفریک ناخالص به دلیل وجود مواد جامد، کلوئیدی و نامحلول به رنگ سبز درمیآید و شکل ظاهری آن شبیه لجن است. برای شفافسازی اسید میتوان آن را تا دمای معینی گرم کرد و بعد با خنک کردن آن و انجام سانتریفیوژ اسید شفافی به وجود آورد. در یکی دیگر از روشها به نام برینش از مواد شفافکننده استفاده میکنند. در یک روش جدیدتر نیز با اضافه کردن آهک به اسید مصرفی در فرایند مرطوب و رسوب دادن یونها، میتوان اسیدی شفاف تولید کرد.
- استخراج حلال ـ حلال: در این روش از حلالهای آلی نامحلول در آب استفاده میکنند که باید قابلیت ایجاد دو فاز غیر قابل امتزاج (فاز اسیدی و فاز ناخالصیها) را داشته باشند.
- روشهای فیزیکی ـ شیمیایی: تولید اسید فسفریک برای گرید خوراکی این روش بسیار مناسب است. این روش با ایجاد شرایط فیزیکی ویژه مانند کنترل دما یا فشار و یا از طریق افزودن مواد شیمیایی خاص ناخالصیها را حذف میکند.
- استفاده از فیلترهای غشائی: با استفاده از این فیلترها میتوان ناخالصیهای فلزی را جدا نمود که با توجه به سایز منافذ و ترکیب شیمیایی غشا نمونه مناسب را باید انتخاب کرد.
- حذف فلزات سنگین: برای بسیاری از کاربردهای این اسید میبایست فلزات سنگین موجود همچون قلع، جیوه و مس را حذف کرد که برای این امر روشهای متفاوتی وجود دارد و باید در این بین روش مناسب را انتخاب کرد. روشهایی مانند: پیرولیز، حذف آرسنیک، حذف لوئور، رنگ بری و… برای خالصسازی اسید فسفریک وجود دارد.
موارد استفاده و کاربردهای اسید فسفریک
استفاده از این اسید به دو صورت اسید فسفریک خوراکی و صنعتی صورت میپذیرد که مهمترین علت آن غیرسمی بودن این اسید است. اگر از طرفداران نوشابهاید، باید بگوییم به مصرف این اسید عادت کردهاید، اما این استفاده تنها محدود به نوشابهها نیست، بلکه در مرباها، پنیرها و گوشتهای فرآوری شده مانند سوسیس و کالباس و غیره، اسید فسفریک کاربردهای فراوانی دارد. این اسید در غذا طعمی تند به خوراکی میدهد.
از کاربردهای جالب این اسید استفاده از آن برای پاک کردن جرمهای دندان در دندانپزشکی است و جالب است بدانید که در خمیردندانهایی که خاصیت سفیدکنندگی دارند نیز استفاده میشود. اگر زمانی خواستید زنگ آهن را پاک کنید انتخاب شما اسید فسفریک خواهد بود. هر چند بعد از استفاده، یک فسفات آهن سیاه خواهید داشت که خود میتواند بهعنوان مادهای ضد خورندگی مورد استفاده قرار گیرد.
بسیاری از مواد شوینده در ساختار خود از اسید فسفریک جهت نرم کردن آب استفاده میکنند. یونهای کلسیم و منیزیم که آب سخت را تشکیل میدهند، توسط این اسید تبدیل به نمک فسفات میشود و باعث عدم رسوب خواهد شد. اما هنوز هم مانند قرن نوزدهم اصلیترین و شاید مهمترین کاربرد اسید فسفریک در تولید کودهای شیمیایی است. فسفر یکی از ضروریترین عناصر جهت رشد گیاهان است و هنوز ۸۰ درصد در کشاورزی مصرف دارد. این کودهای شیمیایی معمولاً بهصورت مونو آمونیوم فسفات، دی آمونیوم فسفات، سوپر فسفات تریپل و فسفات منیزیم هستند.
از کاربردهای جدید این اسید میتوان به تصفیه آب و فاضلاب و نیز مکملهای خوراک دام و طیور نیز اشاره کرد. از این اسید بهعنوان الکترولیت در سلولهای سوختی نیز استفاده شده و از آن برای ساختن دیترجنتهای مصنوعی نیز قابل استفاده است. از این اسید در مواد آرایشی و بهداشتی و مراقبتی نیز استفاده میشود. در ماسکهای اسکراب، لاک ناخن، رنگ مو و پاککنندههای صورت، شامپوهای سر و بدن، از این اسید بهعنوان تنظیمکننده اسیدیته استفاده میشود.

کاربرد اسید فسفریک در صنعت کشاورزی
فسفر یکی از عناصر ضروری در رشد گیاهان است. بخش قابل ملاحظهای از اسید فسفریک تولید شده در تولید کودهای آمونیوم فسفات مصرف میشود. غنی کردن خاکهایی که با فسفات غنی میشوند و باعث رشد سریع گیاهان میشود و افزایش غلظت فسفاتها در سطح آب بر رشد گیاهان آبزی تأثیر مثبت دارد.
وجود کودهای فسفات در آبها و رشد گیاهان آبزی به دلیل وجود آنها، گاهی باعث مرگ گیاهان میشود. گیاهان مرده نیز برای تجزیه شدن از اکسیژن موجود در آب مصرف میکنند و باعث ایجاد خطر در حیات موجودات آبزی میشود. استفاده بیش از حد از کودها برای گیاهان و حتی ریختن فاضلابهای حاوی فسفاتها میتواند برای محیط زیست مشکلاتی را ایجاد نماید و این امر اصول و استاندارهای تعریف شدهای دارد که باید رعایت شود.

اسید فسفریک برای پسته
استفاده از اسید فسفریک در کشاورزی، بهویژه در کشت پسته، به دلیل اهمیت فسفر در رشد و توسعه گیاهان بسیار رایج است. فسفر یکی از عناصر ضروری برای گیاهان است که نقش مهمی در فرآیندهای زیستی مانند تولید انرژی، فتوسنتز و تشکیل ریشههای قوی دارد. اسید فسفریک بهعنوان یک منبع غنی از فسفر، میتواند به بهبود کیفیت و کمیت محصول پسته کمک کند.
مزایای استفاده از اسید فسفریک در کشت پسته:
- افزایش رشد ریشه: فسفر موجود در اسید فسفریک باعث تقویت سیستم ریشهای گیاه پسته میشود، که این امر به جذب بهتر آب و مواد مغذی کمک میکند.
- بهبود گلدهی و تشکیل میوه: فسفر نقش کلیدی در فرآیند گلدهی و تشکیل میوه دارد و استفاده از اسید فسفریک میتواند به افزایش تعداد و کیفیت میوههای پسته کمک کند.
- افزایش مقاومت گیاه: گیاهان با سیستم ریشهای قویتر و تغذیه بهتر، مقاومت بیشتری در برابر تنشهای محیطی مانند خشکی و بیماریها نشان میدهند.
- بهبود کیفیت خاک: اسید فسفریک میتواند به اصلاح pH خاک کمک کرده و شرایط بهتری برای رشد گیاه فراهم کند.
در مجموع، استفاده از اسید فسفریک میتواند به بهبود عملکرد و کیفیت محصول پسته کمک کند، به شرط آنکه بهصورت صحیح و با رعایت نکات ایمنی انجام شود.
کاربردهای اسید فسفریک در پزشکی
اسید فسفریک به دلیل دارا بودن یون هیدروژن فراوان و آلایندگی کمتر نسبت به دیگر اسیدها بهعنوان کاتالیزگر مناسب در ساخت آسپرین استفاده میشود. از دیگر کاربردهای این اسید در پزشکی بهعنوان تمیزکننده و زبر کننده سطح دندان است، بهویژه برای بخشهایی از دندان که وسایل دندانپزشکی با آن سروکار دارد.
از جمله محصولات عرضه شده در زمینه سلامت دندان، خمیر دندان است که در تولید آن از دی کلسیم فسفات، سدیم فسفات، کلسیم پیرو فسفات و تری کلسیم فسفات بهعنوان براقکننده دندان استفاده میشود. علاوه بر خمیر دندان، در دهانشویهها نیز از دی آمونیوم فسفات استفاده میشود.
کاربردهای اسید فسفریک در صنعت
در کنار تمام کاربردهای گفته شده میتوان از کاربرد این ماده در ساخت مدارهای الکتریکی و صنایع الکترونیک نیز نام برد. شرکتها از اسید فسفریک با خلوص بالا به عنوان عامل ایجاد و تهیه مدارهای الکترونیکی در طیف وسیعی از دستگاههای الکترونیکی مانند تلفنهای هوشمند، تلویزیونهای LED و LCD و انواع صفحه نمایش رایانه استفاده میکنند.

کاربرد در صنایع غذایی
اسید فسفریک یکی از افزودنیهای مهم در صنایع غذایی است که به دلیل خواص و ویژگیهای منحصر به فردش، در محصولات مختلف به کار میرود. برخی از کاربردهای اصلی اسید فسفریک در صنایع غذایی عبارتند از:
- تنظیمکننده اسیدیته: اسید فسفریک بهعنوان تنظیمکننده اسیدیته در بسیاری از محصولات غذایی به کار میرود. این اسید میتواند pH محصول را تنظیم کرده و به بهبود طعم و ماندگاری آن کمک کند.
- افزودن طعم تند: در نوشیدنیهای گازدار مانند نوشابهها، اسید فسفریک بهعنوان یک عامل افزودن طعم تند و دلپذیر به کار میرود. این اسید باعث میشود تا نوشیدنیها تازه و شاداب به نظر برسند.
- عامل نگهدارنده: اسید فسفریک با تنظیم pH میتواند به جلوگیری از رشد میکروارگانیسمهای مضر کمک کند و بنابراین بهعنوان یک نگهدارنده در محصولات غذایی استفاده میشود.
- تشکیل کلاتها: اسید فسفریک میتواند با یونهای فلزی موجود در غذا واکنش داده و کلاتهای محلول تشکیل دهد. این عمل باعث تثبیت رنگ و بافت مواد غذایی میشود.
- تقویت مواد معدنی: در تولید محصولات غذایی غنی شده، اسید فسفریک میتواند به عنوان منبع فسفر به کار رود، که یکی از مواد معدنی ضروری برای بدن انسان است. این اسید بهویژه در مکملهای غذایی و غذاهای فرآوری شده استفاده میشود.
- بهبود بافت محصولات غذایی: در صنایع غذایی مانند تولید پنیر، گوشتهای فرآوری شده و سایر محصولات پروتئینی، اسید فسفریک بهعنوان عامل بهبود دهنده بافت به کار میرود. این اسید میتواند به تثبیت ساختار پروتئینها کمک کرده و به بهبود کیفیت نهایی محصول کمک کند.
- پاککنندههای صنعتی: اسید فسفریک در برخی فرآیندهای تمیزکاری و پاککنندگی تجهیزات صنعتی در کارخانههای غذایی به کار میرود. این اسید میتواند رسوبات معدنی و آلودگیها را بهخوبی پاک کند.
در مجموع، اسید فسفریک به دلیل ویژگیهای تنظیمکنندگی، نگهدارندگی و بهبود کیفیت، یکی از افزودنیهای پرکاربرد در صنایع غذایی است که به بهبود طعم، ماندگاری و ارزش تغذیهای محصولات کمک میکند.
دیگر کاربردهای اسید فسفریک
- محصولات مراقبت و نگهداری از خودرو
- باتریها
- پاککنندههای صنایع نیمههادی
- تمیز کردن مبلمان و دیگر محصولات مراقبت
- محصولات الکترونیکی و برقی
- بستهبندیهای غذایی
- سوخت و محصولات مرتبط به آن
- محصولات ظرفشویی و لباسشویی
- محصولات مراقبت و نگهداری از چمن و باغها
- رنگهای ساختمانی و انواع پوشش برای دیوارها
- انواع محصولات کاغذی
- لوازم مورد نیاز برای عکاسی، فیلم و مواد شیمیایی برای ظهور عکس
- محصولات پلاستیکی و لاستیکی
- پاککنندهها و تمیزکنندهها در فرایندهای آبکاری خودرو و ماشینآلات
اسید فسفریک در دندانپزشکی چه کاربردهایی دارد؟
ترکیب پودر روی با اسید فسفریک، فسفات روی را میسازد که به عنوان سیمان دندان در دندانپزشکی استفاده میشود. در زمان ارتودنسی قبل از قرار دادن براکت و سایر وسایل دندانپزشکی برای تمیز کردن میتوان استفاده کرد. برای از بین بردن پلاکها و سفید شدن دندانها با مشتقات این اسید استفاده میشود. ایمپلنتهای فلزی ارتوپدی با فسفات کلسیم پوشانده میشوند تا ادغام آنها با بافت استخوانی را تقویت کنند. سیمانهای فسفاتیک در جراحی سیستمهای استخوانی نیز قابل استفاده است. از نمکهای فسفات برای کاهش درد در دندانهای حساس نیز میتوان استفاده کرد.
دندانپزشکی یکی از اصلیترین زمینههایی است که از اسید فسفریک میتوان استفاده کرد. از این ماده میتوان به عنوان محلول اچینگ استفاده کرد و معمولاً برای تمیز کردن دندانها کاربرد زیادی دارد. از دیگر کاربردهای این ترکیب شامل سفیدکننده دندان یا ترکیب در مایعات شستشوی دهان است. از این ماده در تولید داروهای ضد تهوع نیز میتوان استفاده کرد. از این اسید به عنوان یک الکترولیت در سلولهای سوختی یا ژنراتورهای اکسی هیدروژن استفاده میکنند. این ماده برای ساخت مواد شوینده مصنوعی و تصفیه آب و فلزات نیز استفاده میشود.

موارد استفاده از اسید فسفریک در تصفیه آب
فسفاتها در تصفیه آب آشامیدنی استفاده میشوند. از اسید فسفریک برای جلوگیری از واکنشهای بعدی آبهای زیرزمینی در معرض آهن و منگنز استفاده میکنند که بیشتر به «آب قرمز» و «آب سیاه» معروف هستند. وقتی آهن و منگنز در معرض هوا قرار بگیرند، اکسید شده و رنگ آب را تغییر میدهند. این ترکیب را برای جلوگیری از رسوب مواد معدنی و خوردگی (از pH کم و یا فلزات غیرمشابه) در سیستم توزیع آب استفاده میکنند. این ترکیب سرب و مس محلول را در آب آشامیدنی مصرفکنندگان کاهش میدهد.
خطرات و ایمنی اسید فسفریک
اسید فسفریک زمانی که با پوست تماس پیدا میکند یا در غلظت بالا مصرف شود، بسیار خورنده است و منجر به سوختگی شدید میشود. زمانی که اکسیدکنندههای قوی به اسید فسفریک اضافه میشوند، باعث آتشسوزی یا انفجار میشوند.
اسید فسفریک بسیار خطرناک و سمی است. استفاده در مقادیر کم باعث تحریک پوست، چشم و دستگاه تنفسی میشود. اما اگر بلعیده شود، میتواند آسیب جدی به سیستم گوارشی وارد کند. استنشاق بخار این اسید باعث تحریک دستگاه تنفس میشود. حساسیتهای پوستی و چشمی از جدی خطرات در معرض این اسید قرار گرفتن است.
هنگام استفاده از این ماده باید از دستگاه تنفس معتبر و همچنین از محافظ صورت، دستکش و چکمه استفاده کرد. این اسید را از مواد ناسازگار مانند مواد اکسیدکننده، فلزات، مواد قابل احتراق و قلیاها باید دور نگه داشته شوند و آن را در محلی با تهویه مطبوع و مناسب و به دور از رطوبت در ظروف روکشدار ذخیره کرد.
خرید اسید فسفریک
متقاضیان خرید اسید فسفریک میتوانند با شماره 09354072882 تماس بگیرند و اطلاعات کامل را از شرکت بزرگمهر پارسه دریافت کنند. این شرکت معتبر با ارائه اسید فسفریک با کیفیت بالا، آماده پاسخگویی به نیازهای مختلف صنعتی، کشاورزی و غذایی شما است. برای دریافت مشاوره و اطلاعات بیشتر، لطفاً با کارشناسان شرکت بزرگمهر پارسه تماس حاصل فرمایید.
فروش فسفریک اسید
شرکت بزرگمهر پارسه انواع فسفریک اسید را با کیفیت بالا عرضه میکند. متقاضیان محترم میتوانند برای خرید و دریافت اطلاعات بیشتر با ما تماس بگیرند (شماره تماس: 09354072882). کارشناسان ما آماده ارائه مشاوره و پاسخگویی به تمامی سوالات شما هستند.
نتیجهگیری
اسید فسفریک، که عمدتاً از ترکیب فسفر، اکسیژن و هیدروژن ساخته میشود، یکی از اسیدهای پرکاربرد در صنایع مختلف است. تاریخچه و خواص این اسید، که شامل خصوصیات فیزیکی و شیمیایی منحصر به فردی است، به همراه روشهای تولید و خالصسازی آن بهویژه در کشاورزی، داروسازی و صنایع غذایی اهمیت بسیاری دارد. علاوه بر کاربردهای گسترده در صنعت و پزشکی، باید به نکات ایمنی استفاده از این اسید توجه کرد تا از خطرات احتمالی جلوگیری شود.


