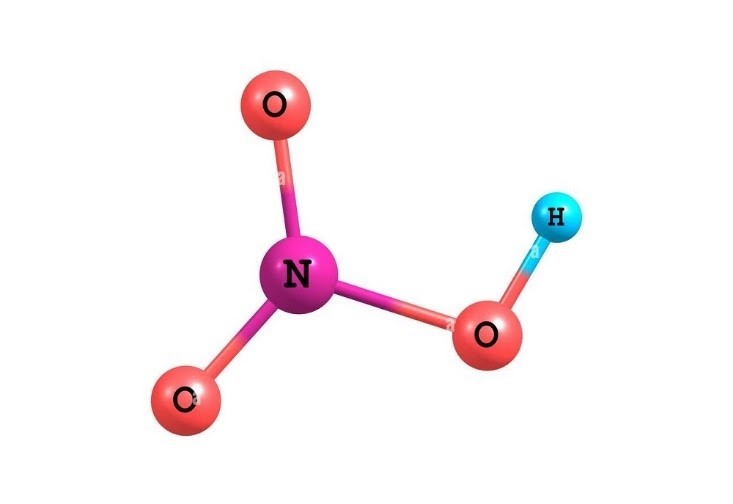
اسید نیتریک مایعی بیرنگ یا زرد رنگ با بویی تند و گزنده یا خفهکننده است. این اسید وقتی در معرض نور قرار میگیرد، تجزیه میشود و دیاکسید نیتروژن (NO2) را تولید میکند که گازی قهوهای رنگ است. رنگ زردی که اغلب در نیتریک اسید مشاهده میشود به دلیل وجود مقادیر کمی از دیاکسید نیتروژن ایجاد میشود. نیتریک اسید بهعنوان یکی از قویترین اکسیدکنندهها شناخته شده است و تقریباً به تمام فلزات بهاستثنای طلا و پلاتین حمله میکند.
خصوصیات نیتریک اسید
اسید نیتریک نامهای دیگری از جمله آکوا فورتیس (آب قوی)، اسید حکاکی و اسید ازتیک دارد. فرمول شیمیایی آن HNO3 است و از عنصرهای هیدروژن، نیتروژن و اکسیژن تشکیل میشود. این ماده نوعی اسید معدنی و به حالت مایع با وزن مولکولی 63.01 گرم بر مول است.
این اسید در 41.6- درجه سانتیگراد ذوب میشود و در 83 درجه سانتیگراد (180 درجه فارنهایت) به جوش میآید. این ماده در این دما که همان نقطه جوش است، تجزیه میشود. این اسید در آب حل و در اتیل الکل تجزیه میشود و با اکثر حلالهای آلی بهشدت واکنش میدهد.
تاریخچه
از گذشته تا کنون این ماده، برای انسانها ارزش فراوانی داشته است. کیمیاگران نیتریک اسید را آکوا فورتیس به معنای «آب قوی» نامیدند. در طول سالیان دراز، انسانهای مختلفی برای شناخت ماهیت این ماده و تولید هرچه بیشتر آن کوشیده و در این راه پیشرفت کردهاند. در ادامه به طور مختصر، به سیر تکامل دانش بشر در رابطه با این ماده میپردازیم.
نیتریک اسید؛ مادهای جذاب و نام آشنا برای دانشمندان
نیتریک اسید قرنهاست که برای دانشمندان شناخته شده است. احتمالاً اولین توصیف از سنتز (تولید) آن در نوشتههای کیمیاگری عربزبان آمده است. این کیمیاگر نامآشنا ابوموسی جابربنحیان (حدود ۷۲۱- حدود ۸۱۵) است که بیشتر با نام لاتین خود «Geber» شناخته میشود. این ماده به طور گسترده توسط کیمیاگران مورد استفاده قرار گرفت، اگرچه آنها چیزی از ترکیب شیمیایی آن نمیدانستند. این رویه تا اواسط قرن هفدهم میلادی ادامه داشت.
پیشرفت فرمولاسیون اسید نیتریک
در قرن هفدهم میلادی شیمیدان آلمانی ژوهان رودولف گلابر (1604-1670) روش بهبودیافتهای برای ساخت اسید نیتریک اختراع کرد. گلابر با افزودن اسید سولفوریک غلیظ (H2SO4) به نمک (نیترات پتاسیم، KNO3) این اسید را تولید کرد. هنوز هم از روشی مشابه برای تهیه نیتریک اسید در آزمایشگاه استفاده میشود، اگرچه این روش ارزش تجاری یا صنعتی کمی دارد یا اصلاً ارزشی ندارد.
ماهیت این ترکیب چه زمانی مشخص و تعیین شد؟
ماهیت شیمیایی و ترکیب نیتریک اسید اولینبار در سال 1784 توسط شیمیدان و فیزیکدان انگلیسی، هنری کاوندیش (1731-1810)، تعیین شد. او یک جرقه الکتریکی روی هوای مرطوب زد و متوجه شد که ترکیب جدیدی تشکیل شده است که همان نیتریک اسید بود. کاوندیش بعدها توانست خواص شیمیایی و فیزیکی این اسید و ترکیب شیمیایی آن را تعیین کند.
روشی که امروزه برای تهیه نیتریک اسید استفاده میشود، روشی است که در سال 1901 توسط شیمیدان آلمانیِ اصالتاً روسی فردریش ویلهلم اوستوالد (1853-1932) ابداع شد. فرایند اوستوالد شامل اکسیداسیون آمونیاک بر روی کاتالیزور پلاتین یا مخلوط پلاتین و رودیوم است.
امروزه نیتریک اسید یکی از مهمترین ترکیبات شیمیایی است که در صنعت استفاده میشود. این ماده رتبه سیزدهم را در بین تمام مواد شیمیایی تولید شده در ایالات متحده در هر سال را دارد. در سال 2005، حدود 6.7 میلیون تن از این ترکیب در ایالات متحده تولید شد.
نحوه تولید نیتریک اسید
اگرچه از نظر تئوری، اسید نیتریک از چندین روش تهیه میشود، تنها یکی از آنها کاربرد تجاری زیادی دارد. این روش اکسیداسیون مستقیم آمونیاک یا همان نسخه بهروز شده و بهبودیافته فرایند سنتی استوالد است. در این روش، آمونیاک گرم میشود و با هوا روی کاتالیزور که معمولاً مخلوطی از فلزات رودیوم و پلاتین است، واکنش میدهد.
این واکنش منجر به تشکیل اکسید نیتریک، گازی بیرنگ به فرمول NO، میشود که سپس به دیاکسید نیتروژن (NO2) تبدیل میشود. دیاکسید نیتروژن با آب واکنش داده و نیتریک اسید را تشکیل میدهد.
موارد مصرف متداول
رایجترین کاربرد نیتریک اسید در ساخت نیترات آمونیوم است که عمدتاً بهعنوان کود مصرف میشود. حدود سهچهارم کل نیتریک اسید تولید شده در ایالات متحده در تولید کودها به کار میرود. دومین کاربرد مهم آن در تولید اسید آدیپیک [COOH(CH2)3COOH] است که حدود 10 درصد از کل نیتریک اسید تولید شده را شامل میشود. این اسید در ساخت نایلون، پلیاورتانها و سایر پلاستیکهای مصنوعی استفاده میشود.
نیتریک اسید برای ساخت انواع نیتراتهای فلزی و برای تمیزکردن فلزات نیز کاربرد دارد. مقادیر کمی از این ترکیب کاربردهای مختلف دیگری دارد. ساخت مواد منفجره و آتشبازی، فرآوری سوختهای هستهای و ساخت انواع خاصی از رنگها، از جمله این کاربردهاست. همچنین بهعنوان شناساگری آزمایشگاهی در آزمایشگاههای تحقیقاتی، تجاری، صنعتی و دانشگاهی عمل میکند. این اسید در حکاکی روی فلزات نیز نقش دارد.
خطرات احتمالی
اسید نیتریک یکی از اجزای باران اسیدی است. باران اسیدی نوعی آلودگی است و زمانی ایجاد میشود که موادی مانند اکسیدهای نیتروژن با آب، اکسیژن و سایر مواد شیمیایی موجود در جو واکنش میدهند. باران اسیدی مضرات زیادی دارد. این نوع باران، میوه، درختان، صیفیجات و گیاهان را آلوده میکند و درنتیجه سلامت انسانها را تحتتأثیر قرار میدهد. باران اسیدی بهمرورزمان به آثار تاریخی صدمه میزند و برای حیوانات نیز بسیار خطرناک است و سبب کوچ زودهنگام پرندگان میشود.
نیتریک اسید یک مادة بسیار سمی است و در نگهداری و استفاده از آن باید موارد ایمنی را رعایت کرد. این اسید به پوست و سایر بافتها حمله کرده و آنها را از بین میبرد و جای زخم زرد رنگی بر جای میگذارد که ناشی از تخریب پروتئینها در پوست یا بافت است. اگر بلعیده، استنشاق، یا بر روی پوست ریخته شود، میتواند عوارض زیادی ایجاد کند که جبرانناپذیر خواهند بود.
از جمله این عوارض سوختگی شدید خورنده در دهان، گلو و معده و تحریک یا سوزش شدید دستگاه تنفسی فوقانی مانند بینی، دهان و گلو است. همچنین، امکان دارد این ماده باعث آسیب به ریهها، مشکلات شدید تنفسی، سوختگی سطح چشم، ورم ملتحمه و کوری شود. در شدیدترین موارد، این اسید ممکن است باعث مرگ فرد شود.
سخن پایانی
اسید نیتریک، (HNO3)، مایع بیرنگ، دودزا و بسیار خورنده است. این ماده کاربردهای فراوانی دارد. این ماده در صنعت و تجارت کاربرد بسیاری دارد و بهعنوان شناساگر آزمایشگاهی نیز عمل میکند. این اسید سمی است و درصورتیکه در زمان استفاده ایمنیهای لازم رعایت نشود ممکن است سوختگی شدید و مشکلات فراوان دیگری به بار بیاورد.